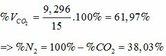Cho 8.4g kim loại sắt tác dụng hết với dung dịch axit clohidric HCL thấy thoát ra V lít khí X (đktc) và dung dịch Y.
a) Tính thể tích khí X sinh ra.
b) Lấy dung dịch Y cô cạn thu được bao nhiêu gam muối.
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).a) Viết phương trình hóa học xảy ra.b) Tính thể tích khí H2 (đktc)
: Cho 19,5g Zinc tác dụng hết với dung dịch có chứa a gam hydrochloric acid HCl, thấy thoát ra V lít khí X và dung dịch Y. Cô cạn dung dịch Y thu được b gam muối.
a. Tính V ở đkc
b. Tìm a , b
a) \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,3--->0,6------>0,3-->0,3
=> V = 0,3.24,79 = 7,437 (l)
b) a = mHCl = 0,6.36,5 = 21,9 (g)
b = mZnCl2 = 0,3.136 = 40,8 (g)
Cho kim loại 14 gam Fe tác dụng với dung dịch axit HCl, thu được dung dịch muối FeCl2và khí H2
a) Viết CTHH xảy ra.
b) Tính khối lượng axit HCl đã dùng.
c) Tính thể tích khí H2 sinh ra ở đktc.
a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Fe}=0,5\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,25.36,5=18,25\left(g\right)\)
c, Theo PT: \(n_{H_2}=n_{Fe}=0,25\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
Cho 7,0 gam hỗn hợp hai muối cacbonat của kim loại hóa trị II tác dụng hết với dung dịch HCl thấy thoát ra V lít khí ở đktc. Cô cạn dung dịch sau phản ứng thu được 9,2 gam muối khan. Giá trị của V là:
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
Đánh máy giúm nha
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ----> ZnCl2 + H2
Mol: 0,1 0,1
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Cho 20,6 gam hỗn hợp muối cacbonat của một kim loại kiềm và một kim loại kiềm thổ tác dụng với dung dịch HCl dư thấy có 4,48 lít khí thoát ra (đktc). Cô cạn dung dịch thu được m gam muối khan. Giá trị của m là
A. 18,4
B. 18,9
C. 22,8
D. 28,8
Đáp án C
nCO2=0.2 nên nHCl=0.4
=> m muối=20.6+0.4*36.5-0.2*44-0.2*18=22.8
Cho 13 gam kẽm Zn vào bình chứa 500ml dung dịch axit clohidric HCL, tác dụng vừa đủ, thu được dung dịch A và v lít khí (đktc).
A. Tính v
B. Tính nồng độ mol/lit của dung dịch axit clohidric HCL đã sử dụng
C. Cô cạn hoàn toàn dung dịch A thu được bao nhiêu gam chất rắn
a) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2--->0,4--->0,2--->0,2
=> V = 0,2.22,4 = 4,48 (l)
b) \(C_{M\left(dd.HCl\right)}=\dfrac{0,4}{0,5}=0,8M\)
c) \(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
cho 44,5 gam hổn hợp bột Zn và Mg tác dụng với dung dịch HCl dư thấy có 4,48lít khí thoát ra ở đktc và dung dịch X . cô cạn dung dịch X thì thu được bao nhiêu gam muối khan ?
Cho 13,8 gam hỗn hợp X gồm kim loại kiềm R và Ca tác dụng hết với nước thu được 5,6 lít H2 (đktc) và dung dịch Y. Mặt khác, cho 8,58 gam kim loại R phản ứng hết với lượng dư dung dịch HCl thì thể tích khí H2 thoát ra lớn hơn 2,24 lít (đktc).
1. Tìm kim loại R?
2. Cho 15 lít hỗn hợp khí Z gồm N2 và CO2 (đktc) vào dung dịch Y. Sau khi phản ứng kết thúc thu được 8,5 gam kết tủa. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp Z?
1.
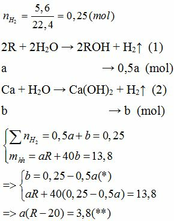
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
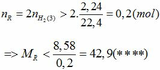
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
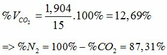
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)